Durante muchos siglos se pensó que el agua, el aire, la tierra y el fuego eran los constituyentes esenciales de toda la materia conocida. Hoy en día y a simple vista sigue pareciendo esta una idea correcta; pero cualquier estudiante de secundaria sabe que se puede profundizar mucho mas en esta idea. A medida que han transcurrido los siglos el caudal del conocimiento humano se ha ido incrementando y lo sigue haciendo día tras día. Por ello lo que se puede decir sobre el agua daría seguramente para escribir mas de un libro. Aquí en todo caso sólo esbozaremos algunas cuestiones muy superficialmente; sobre todo aquellas que pueden resultar curiosas para el público en general.
A simple vista se define, (el agua pura) como un líquido, incoloro, inodoro e insípido o al menos eso creo recordar que me enseñaban en la escuela de mi pueblo en los años 60 del pasado siglo. Lo de que no ha de tener sabor yo pienso que es discutible. Creo recordar que el agua que se utilizaba en las minas para las baterías de las locomotoras eléctricas que era destilada y por tanto no debía tener sabor alguno; no es recomendable para beber;….aunque esto no quiere decir que sea dañina si se bebe (me parece vamos). Quizá el agua destilada es la mas insípida y por ello es menos sabrosa que la que tiene algún componente que le da el sabor agradable. Pero bueno no voy a seguir enredándome con esta cuestión porque me parece que es liar mucho la madeja. Los médicos y farmacéuticos tienen la palabra.
Lo que si tengo más claro es que se definen como aguas potables las que son aptas para el consumo humano. Para ello deben carecer de microbios y tener una cantidad de sales inferior a ciertos límites. Las llamadas aguas duras se definen así por tener excesivo calcio y magnesio (se fija de modo numérico) y son perjudiciales en procesos industriales ya que tienden a obstruir las tuberías.
Las aguas minerales contienen cierta cantidad de nitrógeno, hierro o azufre y se considera que tienen valor terapéutico.
En las escuelas más elementales de nuestros pueblos creo que ya se enseñaba que el agua está formada por hidrógeno y oxígeno. Concretando más cabe añadir que en cuanto al volumen la proporción hidrógeno/oxígeno es de 2 a 1. No obstante en cuanto a peso por cada 8 unidades de oxigeno hay sólo una de hidrógeno. Esto puede parecer contradictorio, pero el mundo está lleno de paradojas y para entender el motivo de todo esto no queda otra que saber un poco más sobre los átomos de hidrógeno y oxígeno que son como las partículas materiales más elementales que forman el agua. Es curioso que a simple vista el agua parece rigurosamente uniforme (muy al contrario que una piedra por ejemplo) y sin embargo ya se sabe desde el siglo XVIII, (Cavendish en 1781) que está formada por dos “cosas” muy distintas. Pues bien vamos a ver como son esas dos cosas.
OXIGENO E HIDROGENO
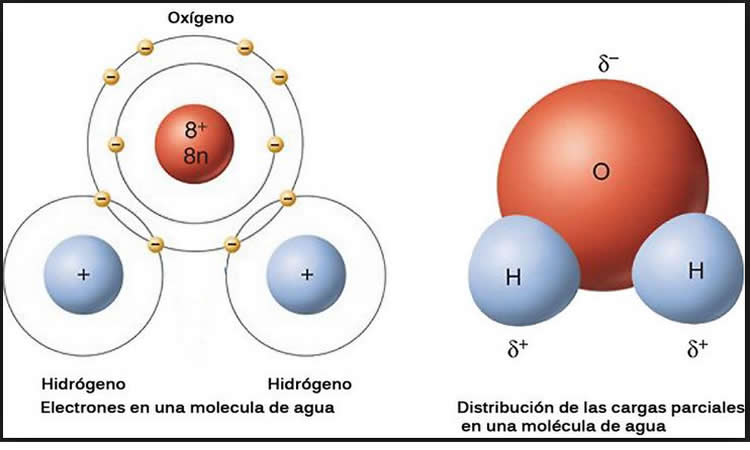
Un átomo de hidrogeno, es como un sistema solar en miniatura, en el que el sol es un protón alrededor del cual está girando un electrón. Es el átomo más sencillo. Por el contrario un átomo de oxígeno es algo más complejo. En su núcleo tiene 8 protones y 8 neutrones, mientras que “los planetas”; serían los 8 electrones que giran en torno al núcleo. La similitud entre el Sistema Solar y un átomo es tal que en éste la masa está concentrada casi en su totalidad en el núcleo, es decir en el “Sol”.
En los libros se dibujan los átomos de hidrógeno y oxígeno del agua de modo que junto a un átomo de oxígeno hay siempre dos de hidrógeno. En la Red, (El camino del agua. Bonsai Menorca. Escuela de Bonsai Antoni Payeras) he localizado unas imágenes que me parecen bien elocuentes. El conjunto de los dos átomos de hidrógeno enlazados a uno de oxígeno es lo que se denomina una molécula de agua.
En esta molécula el radio de la “esfera” de oxígeno es de 1,4 angstrom. Las “esferas” de hidrógeno son más pequeñas, pues su radio es de sólo 0,3 angstrom. Si unimos los centros de estas “esferas” de hidrógeno con la de oxigeno veremos, que forman un ángulo ligeramente superior a los 90 grados, en concreto 104,5 grados sexagesimales. No forman lo que popularmente se llama una “escuadra”. La distancia entre el centro del átomo de oxígeno a los de hidrógeno es de 0,96 angstrom, de lo que cabe deducir que los átomos de hidrógeno y oxígeno están empotrados, tal y como se dibuja en la figura ya señalada de Antoni Payeras. De todos modos al hablar de un átomo no es exacto imaginar a este como una bola de billar. En un átomo la distancia entre el núcleo y sus electrones sólo puede saberse en términos de probabilidad. Los límites reales de un átomo son imprecisos.
Para terminar con este baile de cifras hay que señalar que un angstrom es una unidad de medida que nunca se utiliza en la vida cotidiana; ya que es muy diminuta. En un milímetro caben 10 millones de angstrom. Las medidas en este tipo de unidades se manejan de modo habitual en mineralogía (cristalografía).
En definitiva que cuando nos tomamos un trago de agua fresquita de un manantial, lo que hacemos es ingerir enormes cantidades de “bolitas” que son átomos de hidrógeno y oxígeno, agrupados en moléculas en cada una de las cuales, como reflejan los gráficos adjuntos hay un átomo de oxígeno y dos de hidrógeno (H2O). Por ello el gráfico elegido para acompañar este texto, en vez de ser un arroyo o una fuente es el aludido.
Nunca fui buen estudiante de química pero lo que no aprendí de joven lo intento aprender ahora que ya voy un poco “cascado”,(nunca es tarde), así pues me arriesgué a realizar unos sencillos cálculos en los que espero no haberme equivocado. Partí del hecho de que la cantidad de moléculas de agua que hay en 18 gr.(un mol), son exactamente 6,022 multiplicado por un uno seguido de ¡¡ 23 ceros¡¡. Continuando los cálculos en un vaso cilíndrico de 6 cm. de diámetro y lleno hasta los 5 cm. (un trago normal); tenemos 141,37 gramos de agua; esto es 7,85 moles. En consecuencia el número total de moléculas ha de ser (7,85 x 6,022) = 47,296 pero multiplicado por un uno seguido de 23 ceros. Si ahora queremos saber el número total de átomos multiplíquese por tres el ultimo resultado. Espero no haber “metido la pata”, en el cálculo. Tantos ceros acaban liando a uno.
Rogelio Meléndez Tercero